
以免疫檢查點為目標的癌症治療
Sep 2023 BioLegend x 昶安專欄
以免疫檢查點為目標的癌症治療
2018年諾貝爾生理學和醫學獎,授予發現通過抑制負性免疫調節的方式治療癌症的Dr. James Allison 與Dr. Tasuku Honjo。他們關於T 細胞受體的研究工作始於 1996年,這些受體扮演著剎車的功能,可以阻止 T 細胞殺死癌細胞。他們以動物模式證明,利用針對CTLA-4 (cytotoxic T lymphocyte-associated antigen-4) 和 PD-1 (programmed cell death protein-1) 的單株抗體,可以啟動體內的免疫反應,消除小鼠身上的腫瘤1。這些具有剎車功能的受體現在被稱之為抑制性免疫檢查點(inhibitory immune checkpoint),被視為是免疫。正常情況下負向調節者與正向調節者相互配合,有助於調節T細胞介入的免疫反應。
T細胞介入的免疫反應是一種強大運作機制,可讓T細胞快速擴增、分化和執行功能(圖一)。T細胞的完全激活需要由二種訊號整合而成: 訊號1. T細胞接受器 (T cell receptor; TCR) 辨識由抗原呈現細胞 (antigen presenting cell; APC)表面上的非自我抗原-MHC複合物(圖一)。訊號2. 通過APC表面的共同刺激分子B7-1(CD80)或B7-2(CD86)與T細胞表面的CD28結合2,促使T細胞增生並執行其功能(圖二) 。
BioLegend 昶安獨家代理
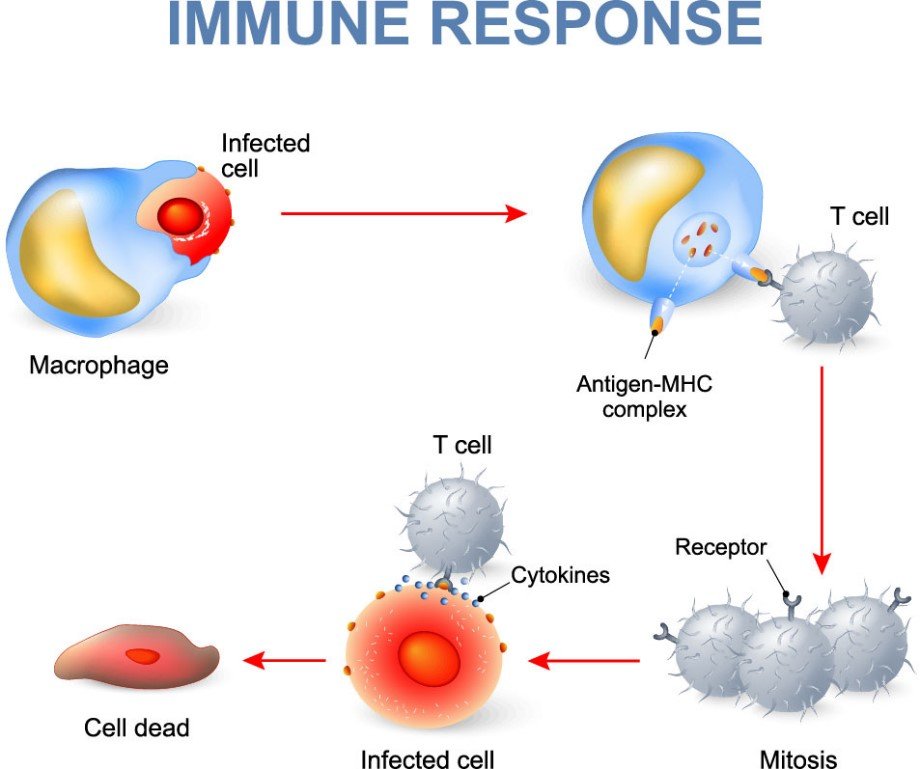
圖一、T細胞根據APC給予的訊號引發相對應的免疫反應。
BioLegend 昶安獨家代理
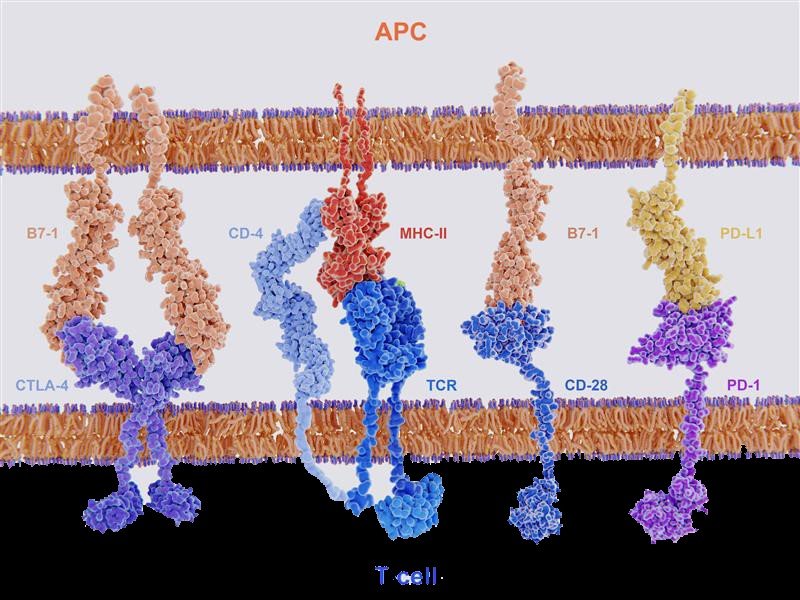
圖二、T 細胞和APC之間配體-受體的交互作用。T細胞激活是在TCR辨識MHC分子後,通過 B7-1與CD28 結合的共同刺激訊號所進行的反應。反之,如果在MHC-TCR辨識後出現來自B7-1與 CTLA-4結合或PD-L1與PD-1結合的共抑制信號,T細胞活性將受到抑制。
BioLegend 昶安科技獨家代理 IL-2 interleukin 2 介白素2
如果訊號2是抑制型的,如抑制性免疫檢查點CTLA-4與B7蛋白結合,則CD28誘發的共同刺激訊息將失效,T 細胞激活也受到抑制(圖二)。CTLA-4和PD-1藉由抑制TCR下游的細胞激素分泌、細胞增生、葡萄糖攝取及代謝,最後導致 T 細胞耗竭3。這種負向免疫調節可以阻止過度的免疫反應,以避免正常組織受損或導致自體免疫3。
然而,我們逐漸了解癌細胞可以透過高表達一些免疫檢查點蛋白,抑制T細胞的作用,逃脫免疫監測,讓腫瘤細胞得以在體內生存3。專一性標靶免疫檢查點蛋白的抗體,可以阻斷 T 細胞與腫瘤細胞相互的結合(圖三),從而釋放T細胞來攻擊腫瘤細胞執行清除作用。現在設計用來針對檢查點蛋白的抗體稱為免疫檢查點抑制劑 (immune checkpoint inhibitors; ICIs)(圖三),是許多產業界的藥物開發的重點方向,並被認為是快速進展的免疫新興療法之一。
BioLegend 昶安科技獨家代理 IL-2 interleukin 2
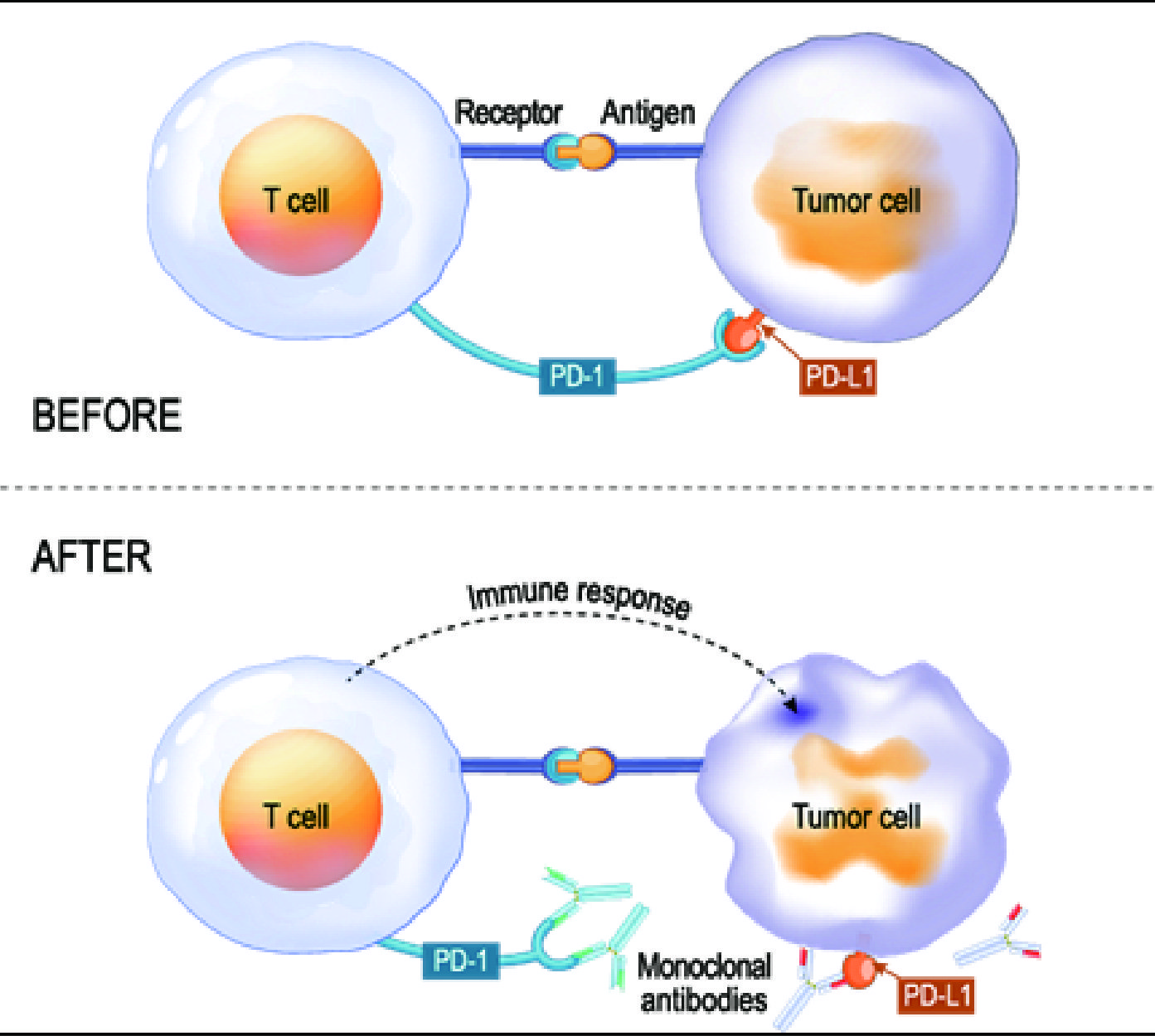
圖三、腫瘤細胞上表現的檢查點蛋白PD-L1和T細胞上表現的PD-1。PD-L1和PD-1間的交互作用可抑制T細胞攻擊腫瘤細胞(上)。 使用PD-1或PD-L1免疫檢查點抑制劑可以啟動T細胞殺死腫瘤細胞(下)。
BioLegend 昶安科技獨家代理 IL-2 interleukin 2
BioLegend 致力於提供值得信賴的專業資源,促進癌症研究和新穎免疫療法的進步。我們的產品組合包括: Avi-tag biotinylated proteins,它提供一致性的標記與蛋白質序列,與未生物素化的蛋白相較下具有相同的生物活性,且不同批次間仍維持其一致的品質。我們針對免疫檢查點提供生物功能重組蛋白和功能性抗體,可用來評估免疫腫瘤學靶標治療的效能,例如已從實驗室基礎研究進展到臨床治療的PD-1、PD-L1和CTLA-4。由於許多患者對於這些特定的ICI治療不具反應性或具有抗藥性,因此推動了開發其他ICI的相關研究。這些ICI可以單獨使用,也可以與抗PD-1/L1和/或抗CTLA-4聯合阻斷,以協同增強抗腫瘤免疫反應5。例如,許多免疫細胞上都表達免疫檢查點共抑制劑-B and T lymphocyte attenuator(BTLA,亦稱之為 CD272) 5。此外,CD80 和 CD86 是與 CD28 相互作用的配體,它們會與CTLA-4 相互競爭,可刺激 T 細胞存活並阻止由CTLA-4引發的抑制T細胞功能。因此,CD80 和 CD86 也被視為標靶治療的目標之一6。目前的治療方法大多是以阻斷抑制性免疫檢查點受體為研究策略,另一種方法則是使用共刺激免疫檢查點受體的類似物,例如腫瘤壞死因子受體超家族 (TNFRSF)的成員-CD40/CD40L7。
研究人員還可以使用我們具有生物活性的GoInVivo™抗體,可以直接透過體內和離體模式測試,確認刺激抗癌免疫反應策略的可行性。這些抗體是針對免疫檢查點標記物而量身訂做,通過功能性驗證測試,批次購買的價格更具競爭力。
精準地量化檢查點分子表達量對於現代生物醫學研究極為重要,幫助我們開發與評估具有潛力的免疫治療。我們的LEGENDplex™ Human Immune Checkpoint Panel 1,這是以流式技術為基礎的多因子檢測法,可同時定量12 種重要的免疫檢查點生物標誌物 (sCD25 (IL-2Ra), 4-1BB, sCD27, B7.2 (CD86), Free Active TGF-β1, CTLA-4, PD-L1, PD-L2, PD-1, Tim-3, LAG-3, and Galectin-9),細胞培養上清液、血清及血漿等樣品已驗證適用於這個分析套組(圖四)。
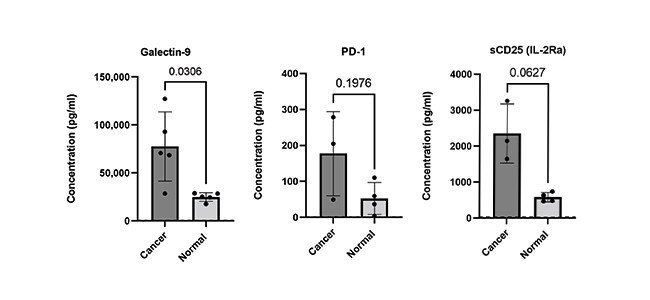
圖四、以LEGENDplex Human Immune Checkpoint Panel 1 (12-plex)分析健康受試者、乳腺癌及肺癌患者血清血漿中的Galectin-9, PD-1及sCD25含量。
BioLegend 昶安科技獨家代理 IL-2 interleukin 2
當今蓬勃發展的免疫療法主要是藉由增強個體自身的免疫系統,精準且有效的消除惡性腫瘤,徹底改變過去對於癌症的治療方式8。與 ICI相似,雙特異性抗體和CAR-T細胞是目前認為最有前瞻性的免疫療法9。今天與大家分享的這篇內容著重於免疫檢查點--細胞表面分子如何調節並影響T細胞功能,腫瘤細胞也利用這個調節機制來逃避免疫監控,開始引發了大家對於ICI的深入研究,這些基礎研究已逐漸轉向臨床,並被認為是許多癌症的標準治療方法。BioLegend的科學家已準備好支持研發,一同協助推動下一代創新療法。
BioLegend 昶安科技獨家代理 IL-2 interleukin 2
參考文獻:
- “Nobel Prizes 2018.” NobelPrize.org, www.nobelprize.org/prizes/medicine/2018/advanced-information/. Accessed 1 Feb. 2023.
- Kuzume, Ayumi et al. “Immune-Checkpoint Blockade Therapy in Lymphoma.” International journal of molecular sciences vol. 21,15 5456. 30 Jul. 2020, doi:10.3390/ijms21155456. PubMed.
- Baldanzi, Gianluca. “Immune Checkpoint Receptors Signaling in T Cells.” International journal of molecular sciences vol. 23,7 3529. 24 Mar. 2022, doi:10.3390/ijms23073529. PubMed.
- Djurian A, Makino T, Lim Y, Sengoku S, Kodama K. Dynamic Collaborations for the Development of Immune Checkpoint Blockade Agents. J Pers Med. 2021 May 24;11(6):460. doi: 10.3390/jpm11060460. PMID: 34073680; PMCID: PMC8225058. PubMed.
- Qin, Shuang et al. “Novel immune checkpoint targets: moving beyond PD-1 and CTLA-4.” Molecular cancer vol. 18,1 155. 6 Nov. 2019, doi:10.1186/s12943-019-1091-2. PubMed.
- Bolandi, Nadia et al. “The Positive and Negative Immunoregulatory Role of B7 Family: Promising Novel Targets in Gastric Cancer Treatment.” International journal of molecular sciences vol. 22,19 10719. 3 Oct. 2021, doi:10.3390/ijms221910719. PubMed.
- Tang, TingTing et al. “Molecular basis and therapeutic implications of CD40/CD40L immune checkpoint.” Pharmacology & therapeutics vol. 219 (2021): 107709. doi:10.1016/j.pharmthera.2020.107709. PubMed.
- Ribas, Antoni, and Jedd D Wolchok. “Cancer immunotherapy using checkpoint blockade.” Science (New York, N.Y.) vol. 359,6382 (2018): 1350-1355. doi:10.1126/science.aar4060. PubMed.
- Mukherjee, Anirban Goutam et al. “Role of Immune Cells and Receptors in Cancer Treatment: An Immunotherapeutic Approach.” Vaccines vol. 10,9 1493. 7 Sep. 2022, doi:10.3390/vaccines10091493. PubMed.


