ENPP1 蛋白在腫瘤微環境中免疫抑制的角色

Ectonucleotide pyrophosphatase/phosphodiesterase 1 (ENPP1) 蛋白已知在軟組織和骨質礦化 (mineralization) 的生理調控中扮演重要的角色。
近年研究發現,ENPP1 蛋白在腫瘤細胞微環境 (tumor microenvironment) 中更有一直先天免疫反應 (innate immunity) 與促進腫瘤細胞生長與轉移 (tumor progression and metastasis) 的作用,成為新興抗癌標靶開發的重點蛋白 (1-2)!
ENPP1 蛋白對於旁分泌 STING 訊號傳遞路徑的抑制作用
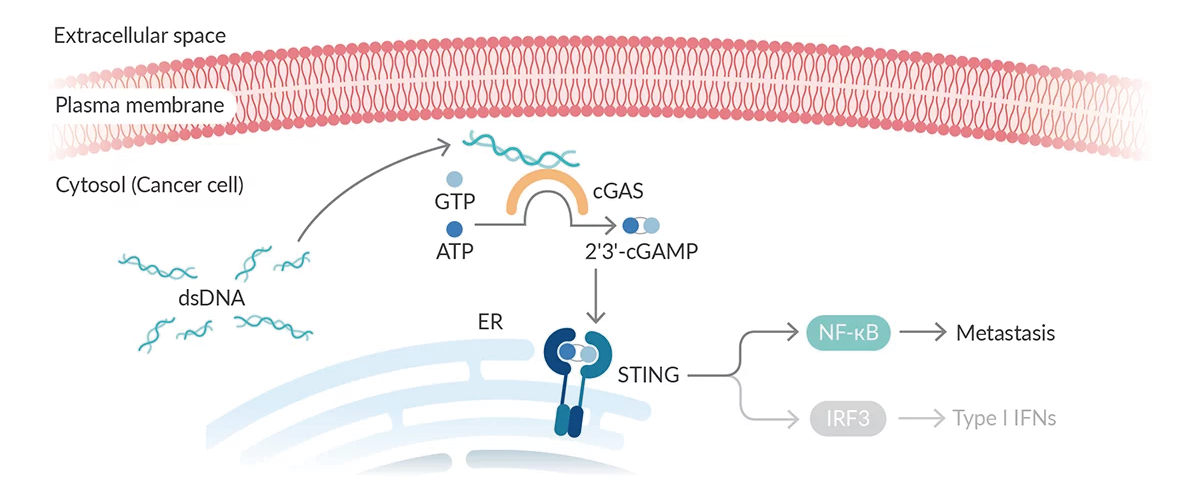
在癌症細胞中,染色體的不穩定促使微核 (micronuclei) 的生成,導致雙股 DNA (double-stranded DNA, dsDNA) 滲出至細胞質中 (2-3)。在細胞質中,這些 dsDNA 進一步被DNA調控系統中的環鳥苷酸-腺苷酸合成酶 (cyclic GMP-AMP synthase, cGAS) 辨識出來,誘導2'3'-cyclic GMP-AMP (2'3'-cGAMP) 的生成 (Fig.1).
而2'3'-cGAMP作為免疫刺激的第二信使,進一步與干擾素刺激因子 (stimulator of interferon genes, STING) 結合並將其活化,從而促使下游轉錄因子:IRF3和NF-κB的磷酸化,引起第一型IFN促發炎細胞因子的分泌 (4)。
腫瘤細胞中染色體的不穩定性,引導下游STING 路徑更偏向於 NF-Κb誘導的免疫反應,造成dsDNA 的損傷,降低腫瘤細胞的轉移 (2)。
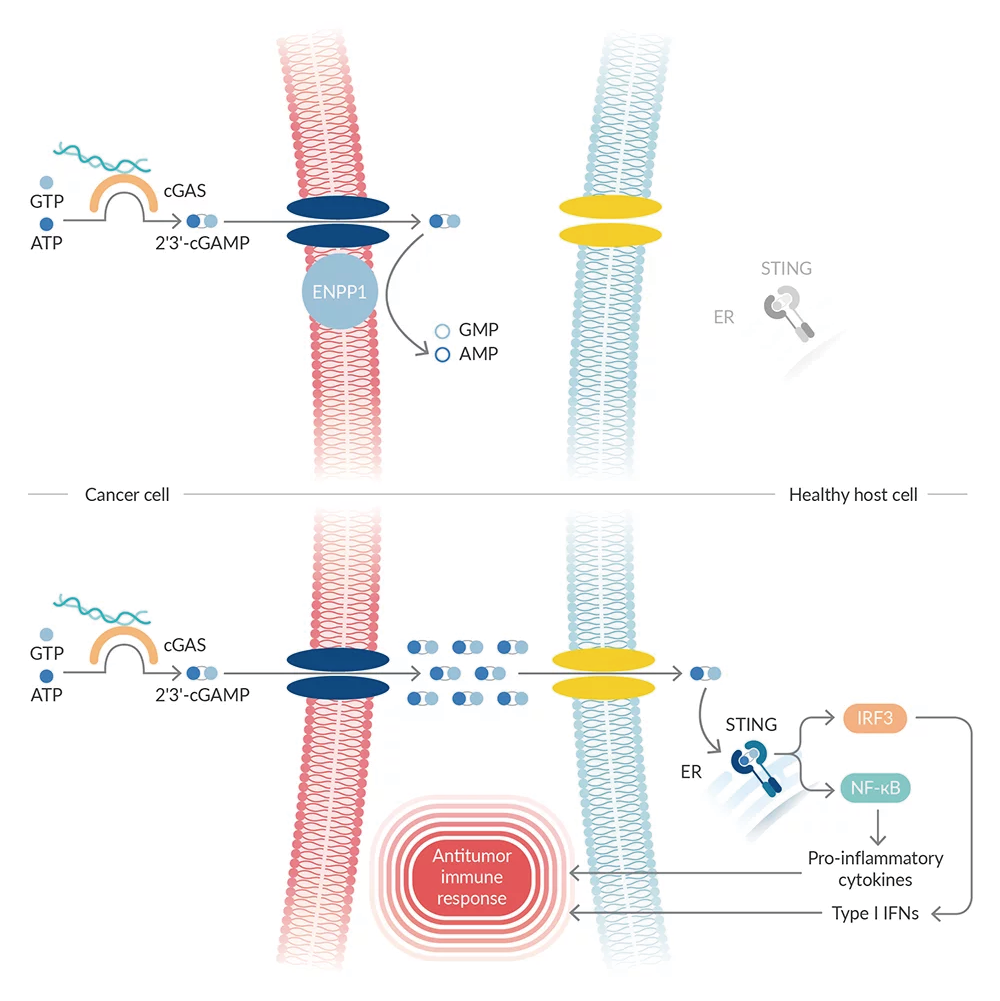
腫瘤細胞將溶解度高的2'3'-cGAMP 輸出到細胞質外,附近的宿主細胞 (host cell) 將其吞噬,進而活化典型 STING 訊號傳遞路徑 (canonical STING signaling),加劇免疫反應。這一系列的免疫反應包含了:第一型 IFN 的生成、樹突狀細胞聚集 (dendritic cell recruitment) 以及毒殺型T細胞的活化 (Fig.2),進一步惡化癌症疾病的進程 (2-3,5)。
反之,ENPP1 蛋白可以透過減弱上訴免疫風暴的訊號傳遞,改善預後不良的狀況 (2,5-6) 。
常見的癌症路徑包含:卵巢癌 (ovarian)、乳癌 (breast cancer)、肝癌 (HCC)、甲狀腺癌 (thyroid cancer) 以及胰臟癌 (pancreatic cancer) 等 (2,5-6)。
ENPP1 蛋白是一種穿膜蛋白 (transmembrane protein),具有面向外部的催化結構域 (external-facing catalytic domain) 能夠將2'3'-cGAMP降解,進而抑制腫瘤微環境中,旁分泌STING訊號的傳遞。
透過這個機制可以有效的削弱免疫反應 (3,7)。
也只有在細胞外的2'3'-cGAMP降解時,能夠抑制腫瘤細胞的免疫活化反應,更能夠減少腫瘤細胞轉移的情況發生 (3)。
ENPP1蛋白在腺苷 (adenosine) 訊號傳遞的貢獻
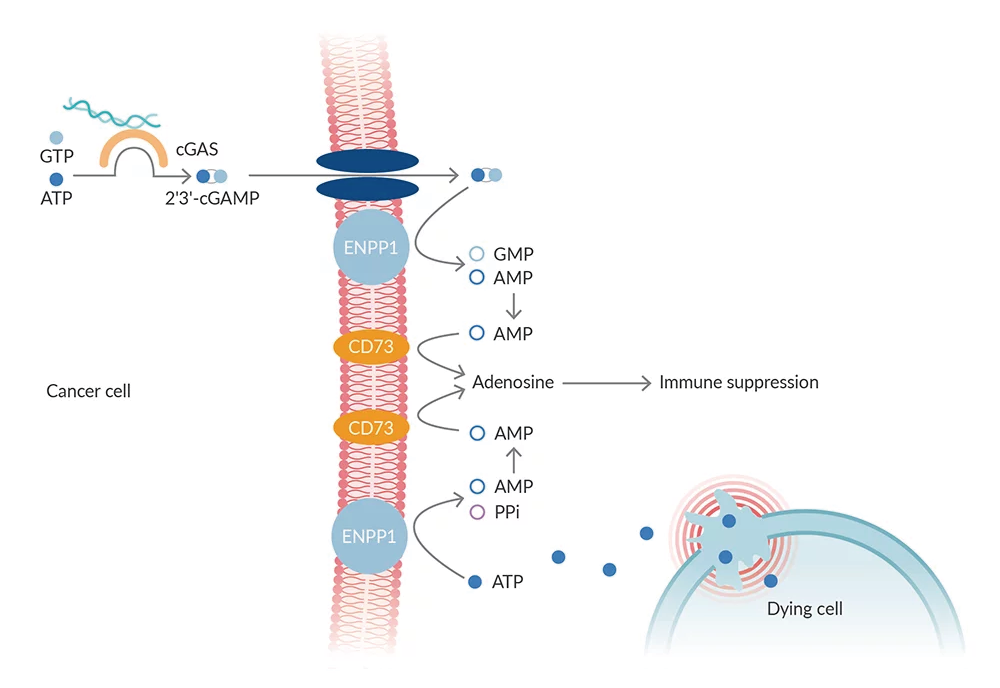
ENPP1 蛋白在免疫脫逃 (immune evasion)中具有輔助的作用,協助腺苷(adenosine) 的生成。上著提到, ENPP1蛋白可以把2'3'-cGAMP水解,形成 GMP和 AMP (7)。ENPP1 蛋白同時也可以水解 ATP (Fig.3)。在ATP水解的過程中,同時也意味著腫瘤微環境壓力的增加。因為細胞損傷和凋亡不停地發生,並且促進發炎反應的發生,進而產出AMP和無機焦磷酸鹽 (inorganic pyrophosphate, PPi)。
AMP 的兩大來源:2'3'-cGAMP水解和ATP水解所得。
AMP進一步被ecto-5'-nucleotidase (NT5E; CD73) 水解,形成腺苷,與細胞外的腺苷受體結合,抑制促發炎細胞因子的生成分泌,促進抗發炎細胞因子的分泌,促進細胞遷移 (cell migration),並促進腫瘤細胞的生長 (2,7)。
透過降解 ATP和 2'3'-cGAMP, ENPP1 蛋白不單抑制了促發炎的狀況,更刺激腺苷的分泌。而腺苷具有免疫抑制的功能性。
推薦產品:
| 702090 | 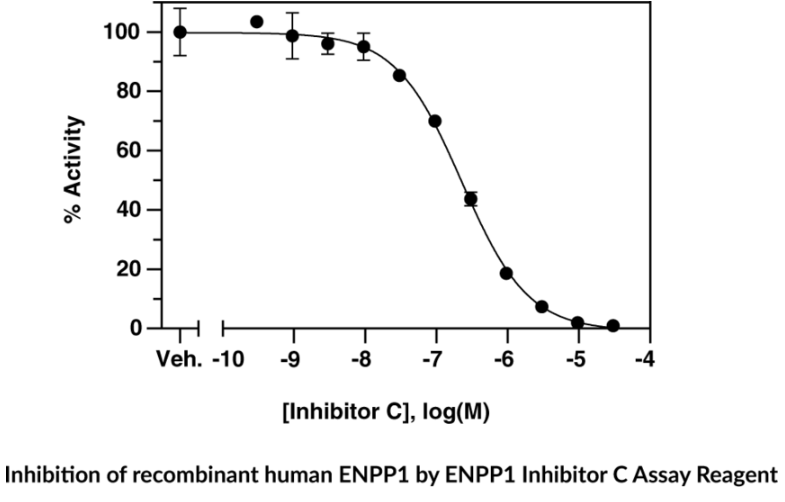 |
| 501700 | 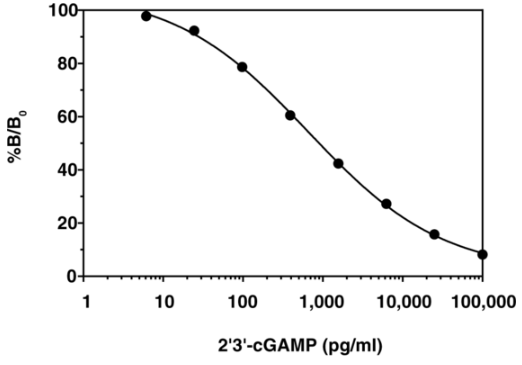 |
ENPP1 蛋白作為癌症治療的重點
References
1. Roberts, F., Zhu, D., Farquharson, C., et al. ENPP1 in the regulation of mineralization and beyond. Trends Biochem. Sci. 44(7), 616-628 (2019).
2. Li, J., Duran, M.A., Dhanota, N., et al. Metastasis and immune evasion from extracellular cGAMP hydrolysis. Cancer Discov. 11(5), 1212-1227 (2021).
3. Carozza, J.A., Brown, J.A., Böhnert, V., et al. Structure-aided development of small-molecule inhibitors of ENPP1, the extracellular phosphodiesterase of the immunotransmitter cGAMP. Cell Chem. Biol. 27(11), 1347-1358 (2020).
4. Kumar, M. and Lowery, R.G. Development of a high-throughput assay to identify inhibitors of ENPP1. SLAS Discov. 26(5), 740-746 (2021).
5. Carozza, J.A., Böhnert, V., Nguyen, K.C., et al. Extracellular cGAMP is a cancer-cell-produced immunotransmitter involved in radiation-induced anticancer immunity. Nat. Cancer1(2), 184-196 (2020).
6. Wang, H., Ye, F., Zhou, C., et al. High expression of ENPP1 in high-grade serous ovarian carcinoma predicts poor prognosis and as a molecular therapy target. PLoS One 16(2), e0245733 (2021).
7. Onyedibe, K.I., Wang, M., and Sintim, H.O. ENPP1, an old enzyme with new functions, and small molecule inhibitors – a STING in the tale of ENPP1. Molecules 24(22), 4192 (2019).
8. Weston, A., Thode, T., Munoz, R., et al. Abstract 3077: Preclinical studies of SR-8314, a highly selective ENPP1 inhibitor and an activator of STING pathway. Cancer Res. 79(13 Suppl), 3077 (2019).
9. Weston, A.S., Thode, T.G., del Villar, R.R., et al. Abstract LB-118: SR8541A is a potent inhibitor of ENPP1 and exhibits dendritic cell mediated antitumor activity. Cancer Res. 80(16 Suppl), LB-118 (2020).
10. Baird, J., Dietsch, G., Florio, V., et al. MV-626, a potent and selective inhibitor of ENPP1 enhances STING activation and augments T-cell mediated anti-tumor activity in vivo. Society for Immunotherapy of Cancer 2018 Annual Meeting Posters. 7 (2018).
更多資訊,請洽 Cayman 台灣代理 - 昶安科技。